Сторінка
1
Будова, властивості глюкози і сахарози. Властивості крохмалю.
ДОСЛІД 1. Взаємодія глюкози з дигідроксидом міді і оксидом срібла.
ХІД ДОСЛІДУ 1: У пробірку налийте 1 мл, розчину глюкози, прилийте стільки ж розчину їдкого натру. До суміші добавте 4-5 крапель розчину сульфату міді і нагрійте до кипіння. Поясніть свої спостереження. Складіть рівняння реакції. Повторіть у такій самій послідовності дослід із сахарозою.
Який висновок на підставі спостережень можна зробити?
2. У пробірку налийте 5 мл розчину лугу і кип’ятіть 1-2 хв. Після цього розчин вилийте, а пробірку старанно промийте дистильованою водою. У підготовлену пробірку влийте 0,5-1 мл. аміачного розчину оксиду срібла і 1-2мл розчину глюкози. Суміш, не збовтуючи, нагрійте на водяній бані або на слабкому полум’ї газового пальника. Що спостерігається? На що вказує — цей дослід? Яка функціональна група входить до складу молекули глюкози. Повторіть у такій самій послідовності дослід з сахарозою.
ДОСЛІД 2. Взаємодія сахарози з гідроксидом кальцію.
ХІД ДОСЛІДУ: В пробірку налийте 3 мл. розчину сахарози, долийте приблизно 2 мл вапняного молока. Що спостерігається? Через розчин пропустіть діоксид вуглецю. Які зміни відбулися в розчині?
Сахароза, я складі молекули якої є кілька гідроксильних груп, подібно багатоатомним спиртам вступає в реакцію s гідроксидами, утворюючи похідні дисахаридів типу алкоголятів - так звані сахарати, Сахарати добре розчиняються у воді. Сахарат кальцію - нетривка сполука: під дією діоксиду вуглецю із сахарату виділяється вільна сахароза, а гідроксид кальцію осаджується діоксидом вуглецю у вигляді дрібнокристалічного карбонату кальцію,
ДОСЛІД 3. Взаємодія крохмального клейстеру з йодом.
ХІД ДОСЛІДУ: Налийте півпробірки води і всипте у дистильовану воду близько 0,2г, крохмалю. Суміш добре збовтайте, вилийте в посудину з 50 мл. киплячої дистильованої води і старанно перемішайте. Влийте 3-4 мл крохмального клейстеру в пробірку, охолодіть і прилийте 1 мл йодної води. Що спостерігається? Нагрійте рідину в пробірці до кипіння і знову охолодіть. Як змінилася рідина?
ДОСЛІД 4. Гідроліз крохмалю,
ХІД ДОСЛІДУ: В 6 пробірок до половини їх об’єму налийте дистильованої води, в кожну пробірку капніть по 2-3 краплі розчину йоду. Близько 2 г крохмалю збовтайте в пробірці з 10 мл дистильованої води, і вилийте в колбочку з 100 мл киплячої дистильованої води. Розчин добре перемішайте. До утвореного крохмального клейстеру добавте 2 мл розчину сірчаної кислоти.
3-4 краплі суміші перенесіть у першу пробірку з розчином йоду і суміш збовтайте. Потім закріпіть колбу в штативі закріпіть колбу в штативі і кип’ятіть рідину. Через кожні 2 хв. переносьте до 3-4 краплі суміші в одну із пробірок з водним розчином йоду і перемішуйте суміш з пробірках.
При нагріванні крохмалю з розбавленою сірчаною кислотою крохмаль поступово гідролізується.
Схему гідролізу крохмалю можна зобразити так:
(С6Н10О5)х à (С6Н10О5)n à (С6Н10О5)m
розчинний декстрин
крохмаль
à p С12Н22О11 à 2p С6Н12О6.
мальтоза глюкоза
Скорочено: (С6Н10О5)х + хН2О à xС6Н12О6.
Iз збільшенням ступеня гідролізу спостерігається поступова зміна забарвлення розчину йолу від внесення кожної наступної проби гідролізату.
Висновки:
В-1
1. Яким чином зображають макромолекулу полімеру. Зобразити двома способами формулу поліетилену, поліхлорвінілу.
2. Номенклатура і класифікація полімерів.
3. Які полімери називають змитими. Ряд фізико-хім. властивостей в залежності від будови макромолекул. Новести приклади різних типів приєднання в макромолекулі.
В-2
1. Дати визначення поняттям “мономер”, “олігомер”, “полімер”.
2. Яку будову може мати макромолекула полімеру? Пояснити на конкретних прикладах.
3. Класифікація за будовою основного ланцюга. Насичені і ненасичені карболанцюгові полімери. Навести 5 прикладів різних карболанцюгів полімерів.
В-3
1. Які полімери називають регулярними, нерегулярними, стереорегулярними. Типи стереорегулярних полімерів. Пояснити на прикладах поліпропілену.
2. На прикладі полі вінілового спирту покажіть просторову будову макромолекули полімеру.
3. Класифікація за поширенням у природі і за будовою макромолекули.
В-4
1. Дати визначення поняттям “макромолекула”, “складова ланка”, “ступінь полімеризації”.
2. Який з полімерів має кращі фізико-механ. властивості: синдіотоктичний чи атактичний поліпропілен ?
3. Як побудовані гетероланцюгові полімери, їх поділ. Навести по 3 приклади.
№1
1. Що таке – цис ізомери і – транс ізомери. Навести приклади ненасичених вуглев.
2. За неведеними схемами напишіть рівняння реакції і вкажіть продукт реакції і до яких груп вони відносяться?
а) СН ![]() СН + НСl
СН + НСl ![]()
б) С4Н6 + О2 ![]()
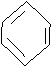 в)
в)
+ Н2 ![]()
3. Назвіть за систематичною номенклатурою такі сполуки.
а) С4Н9 С2Н5 СН3
![]()
![]()
СН2 – С – С = С – С – СН2 – СН2
![]()
![]()
![]()
![]()
![]()
